d-α-토코페릴호박산
d-α-Tocopheryl Acid Succinate

분자식: C33H54O5
분자량: 530.79
이 명: RRR-α-Tocopheryl acid succinate
CAS No.: 4345-03-3
함 량 이 품목은 d-α-토코페릴호박산(C33H54O5)으로서 96.0~102.0%를 함유한다.
성 상 이 품목은 백~회백색의 결정성분말이다.
확인시험 (1) 순도시험 중 (3) 비선광도의 시험용액 10mL에 질산 2mL를 가하고, 저으면서 혼합하여 75℃에서 약 15분간 가열하면 선명한 적~주황색을 나타낸다.
(2) 정량법에 따라 얻은 크로마토그래피의 주된 피크는 내부표준물질의 위치와 비교할 때 표준용액의 피크와 동일한 위치를 나타낸다.
순도시험 (1) 산도 : 이 품목 1g을 0.1N 수산화나트륨용액으로 중화시킨 알콜 및 에테르의 동량 혼합액 25mL에 녹이고 페놀프탈레인시액 0.5mL를 가하고 0.1N 수산화나트륨용액으로 엷은 홍색이 30초간 유지될 때까지 적정할 때, 그 소비량은 18.0~19.3mL이어야 한다.
(2) 납 : 이 품목 약 10g을 정밀히 달아 도가니 또는 백금접시에 넣고 25% 황산 5mL를 주의하면서 가해주고 잘 섞은 다음 수욕조에서 증발건고한 후에 열판위에서 천천히 대부분의 황산이 없어질 때까지 예비회화를 한 후 450~550℃에서 회화한다. 회화가 불충분할 때는 상기 조작을 되풀이 한다. 따로 25% 황산 5mL를 이용하여 같은 방법으로 공시험용액을 조제한다. 회화가 끝나면 1N 염산 5mL를 가하여 수욕조에서 건고한 다음 3N 염산 1mL 및 물 약 5mL를 가하여 잔류물을 용해한 후 물을 가하여 10mL로 하고 측정 농도에 맞게 희석한 액을 시험용액으로 하여 원자흡광광도법 또는 유도결합플라즈마발광광도법에 따라 시험할 때, 그 양은 2.0ppm 이하이어야 한다.
(3) 비선광도
시험용액의 조제 : 이 품목을 α-토코페롤로서 200mg에 상당하는 양을 취하여 유리마개가 달린 250mL의 환저플라스크에 넣고 무수알콜 50mL로 녹여 1분 동안 환류 시킨다. 이 용액을 끓이는 동안 과열되는 것을 방지하기 위해 냉각관을 통해 천천히 알갱이의 수산화칼륨 약 1g을 가하여 20분 동안 환류한 후 식히지 않고 냉각관을 통해 2mL의 염산을 한 방울씩 가한다. (염산을 첨가하는 것은 알칼리 상태의 시료가 공기 중에 산화되는 것을 방지하기 위한 것이다.) 이어서 용액을 식힌 다음 500mL 분액깔때기에 넣고 물과 에테르를 각각 100mL씩으로 용액이 들어있던 플라스크를 씻어 분액깔때기에 합쳐 세게 흔든 후 정치하여 각각의 층을 분취한다. 물층은 다시 50mL의 에테르로 2회 추출하여 따로 분리해 놓은 에테르층에 합한다. 에테르층은 물 100mL로 4회 씻어준 후 에테르를 수욕상 또는 질소가스로 7~8mL로 될 때까지 농축한다. 남아있는 에테르는 상온에서 모두 날려 보내고 즉시 잔류물에 2N 황산•에탄올의 혼액(1 : 72)으로 녹여 200mL로 한 액을 시험용액으로 한다.
시험방법 : 이 품목을 α-토코페롤로서 약 100mg에 상당하는 양을 취하여 분액깔때기에 넣고 물 200mL를 가하여 녹인다. 에테르 75mL로 추출한 다음 다시 에테르 25mL로 2회 추출한 액을 다른 분액깔때기에 합한다. 여기에 수산화나트륨용액(1→125)의 10% 페리시안화칼륨용액 20mL를 가하여 3분간 흔든다. 에테르용액은 물 50mL로 4회 씻고 물층은 버리고 다시 무수황산나트륨으로 탈수시킨다. 에테르용액은 수욕상 또는 질소가스로 7~8mL로 될 때까지 농축하고 남은 에테르 용액은 상온에서 날려 보낸다. 즉시 잔류물을 이소옥탄 5mL를 가하여 녹인 후 선광도측정법에 따라 비선광도시험을 할 때 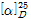 =+24° 이상이어야 한다.
=+24° 이상이어야 한다.
정 량 법
시액 및 용액
내부표준용액 : 헥사데실헥사데카노에이트를 n-헥산에 녹여 3mg/mL로 조제한다.
표준용액의 조제 : d-α-토코페릴호박산 표준품 30mg을 정밀히 달아 약 15mL의 마개달린 병에 취하고, 여기에 메탄올 2mL, 2,2-디메톡실프로판 1mL 및 염산 0.1mL을 넣어 잘 섞어준 다음 1시간 동안 암소에 방치한 후 수욕조에서 질소를 흘려주어 증발건고한다. 이어서 내부표준용액 10mL를 가하여 뚜껑을 닫고 강렬하게 흔들어 녹인 후 표준용액으로 한다.
시험용액의 조제 : 이 품목을 d-α-토코페릴호박산 약 30mg에 상당하는 양을 정밀히 달아 표준용액의 조제에서와 같이 동일하게 한다.
조작조건
칼 럼 : HP-1(30m×0.32mm) 또는 이와 동등한 것
검 출 기 : 수소염이온화검출기(FID)
주입구온도 : 290℃
칼럼온도 : 260~280℃의 일정온도
검출기온도 : 300℃
캐리어가스 : 질 소
장치의 적합성 : 검량선의 방법에 따라 n-헥산 mL당 α-토코페롤표준품과 α-토코페릴아세테이트표준품 각각 1mg을 여러번 주입하여 헥사데실데카노에이트의 지연시간에서 생기는 주피크간의 분리능[R]을 확인한다.
검 량 선 : 3회 연속하여 주입한 상대반응계수가 일정하게(2% 범위 내에서)될 때까지 각각의 표준용액 2~5μL를 연속적으로 주입한다. 대략 지연시간 1.99의 유도체화된 표준품인 메틸 α-토코페릴 호박산(AS)과 지연시간 1.0의 헥사데실헥사데카노에이트(AI)의 넓이를 측정하고 그 값을 각각 AS와 AI이라 한다.
다음 계산식에 의해 표준용액의 각 농도에 대해 계수 “F”를 구한다.
F
=
AS
×
CI
AI
CS
CI : 내부표준용액의 정확한 농도(mg/mL)
CS : d-α-토코페릴호박산 표준용액의 정확한 농도(mg/mL)
시험조작 : 검량선의 방법에 따라 시험용액 2~5μL를 주입하고 지연시간 1.99의 메틸 α-토코페릴호박산과 1.0의 헥사데실헥사데카노에이트에 나타나는 주피크의 면적 aU, aI을 각각 구한 다음 계산식에 따라 검체 중의 d-α-토코페릴호박산의 함량(%)을 계산한다.
d-α-토코페릴호박산(%)
=
10CI
×
aU
×
100
F
aI
검체의 채취량(mg)

분자식: C33H54O5
분자량: 530.79
이 명: RRR-α-Tocopheryl acid succinate
CAS No.: 4345-03-3
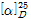 =+24° 이상이어야 한다.
=+24° 이상이어야 한다.F
=
AS
×
CI
AI
CS
d-α-토코페릴호박산(%)
=
10CI
×
aU
×
100
F
aI
검체의 채취량(mg)
